1 材料与方法
1.1 蜱类采集
1.2 蜱种鉴定
1.2.1 形态学鉴定
1.2.2 分子生物学鉴定
表1 本研究采集蜱种类鉴定及其携带病原体PCR扩增的引物序列及反应条件Tab. 1 Primer sequences and reaction conditions for PCR amplification for tick species identification and pathogen detection |
| 目标物种 | 目标基因 | 引物序列(5′-3′) | 扩增序列长度(bp) | 反应条件 | 参考文献 |
| 蜱 | 16S rRNA基因 | Forward1:CTGCTCAATGATTTTTTAAATTGCTGTGG | 460 | 94 ℃5 min;92 ℃30 s,54 ℃30 s,72 ℃30 s,37个循环;72 ℃8 min | [16] |
| Reverse1:CCGGTCTGAACTCAGATCAAGT | |||||
| 巴贝虫 | SUU rRNA基因 | Forward1:GTCTTGTAATTGGAATGATGG | 450 | 94 ℃5 min;94 ℃45 s,55 ℃50 s,72 ℃1 min,40个循环;72 ℃5 min | [17] |
| Reverse1:TAGTTTATGGTTAGGACTACG | |||||
| 无形体 | 16S rRNA基因 | Forward1:TTGAGAGTTTGATCCTGGCTCAGAACG | 450 | 94 ℃5 min;94 ℃45 s,55 ℃50 s,72 ℃1 min,40个循环;72 ℃5 min | [18] |
| Reverse1:CACCTCTACACTAGGAATTCCGCTATC | |||||
| Forward2:TTGAGAGTTTGATCCTGGCTCAGAACG | |||||
| Reverse2:GTACCGTCATTATCTTCCCTA | |||||
| 贝纳柯克斯体 | com1 | Forward1:GCTGTTTCTGCCGAACGTAT | 526 | 94 ℃5 min;92 ℃30 s,56 ℃30 s,72 ℃30 s,37个循环;72 ℃5 min | [19] |
| Reverse1:AGACAACGCGGAGGTTTTTA | |||||
| 伯氏疏螺旋体 | 5S-23S rRNA基因 | Forward1:ACCATAGACTCTTATTACTTTGAC | 380 | 94 ℃5 min;92 ℃30 s,58 ℃30 s,72 ℃30 s,37个循环;72 ℃5 min | [20] |
| Reverse1:TAAGCTGACTAATACTAATTACCC | |||||
| Forward2:ACCATAGACTCTTATTACTTTGACCA | 225 | 94 ℃5 min;92 ℃30 s,52 ℃30 s,72 ℃30 s,37个循环;72 ℃5 min | |||
| Reverse2:ACCATAGACTCTTACTTTGAC | |||||
| 马泰勒虫 | 18S rRNA基因 | Forward1:TTTGGGCTGTTTACAGTTGC | 531 | 94 ℃5 min;92 ℃30 s,60 ℃30 s,72 ℃30 s,37个循环;72 ℃5 min | [21] |
| Reverse1:CTCAAAGTAAACGTCGAGTCATG |
注:SUU rRNA核糖体小亚基rRNA(ribosomal small subunit rRNA,SSU rRNA)。 |
1.3 病原体检测
1.4 进化分析
2 结果
2.1 采获蜱种及数量
表2 新疆维吾尔自治区塔什库尔干塔吉克自治县蜱采样结果Tab. 2 Tick sampling results in Taxkorgan Tajik Autonomous County, Xinjiang Uygur Autonomous Region |
| 蜱种类 | 金草滩湿地 | 斯如依沟 | 提孜那甫 | 库克西鲁克 | 盘龙古道 | 总计 | |||||||||
| 雌 | 雄 | 雌 | 雄 | 雌 | 雄 | 雌 | 雄 | 雌 | 雄 | ||||||
| 寄生蜱 | |||||||||||||||
| 丹氏血蜱 | 17 | 4 | 27 | 5 | 69 | 11 | 18 | 3 | 0 | 0 | 154 | ||||
| 胫距革蜱 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ||||
| 具沟血蜱 | 6 | 2 | 38 | 12 | 17 | 4 | 10 | 6 | 0 | 0 | 95 | ||||
| 游离蜱 | |||||||||||||||
| 丹氏血蜱 | 0 | 0 | 56 | 44 | 0 | 0 | 0 | 0 | 7 | 5 | 112 | ||||
| 胫距革蜱 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 1 | 2 | ||||
| 具沟血蜱 | 0 | 2 | 13 | 15 | 0 | 0 | 3 | 0 | 0 | 0 | 33 | ||||
| 合计 | 23 | 8 | 134 | 76 | 86 | 15 | 31 | 9 | 8 | 6 | 396 | ||||
2.2 病原体检测
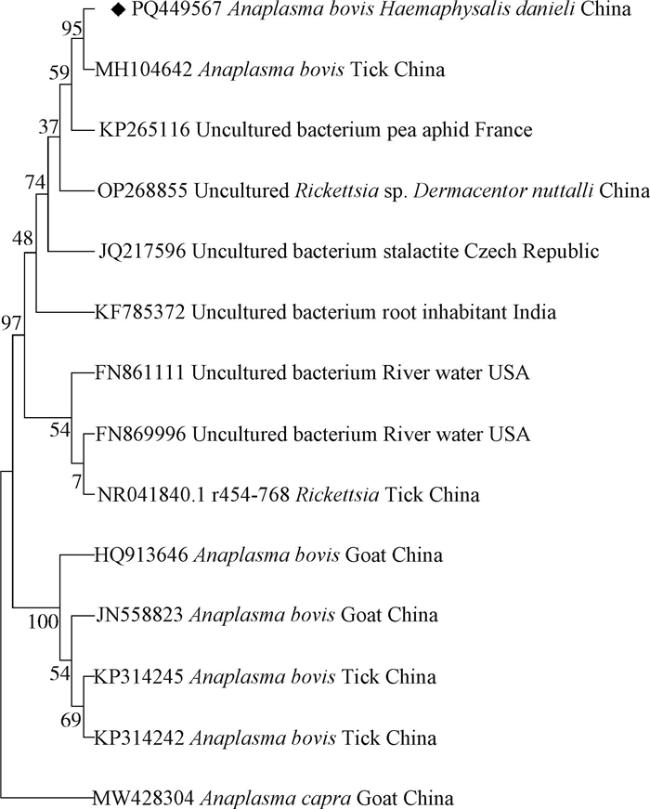
图2 基于16S rRNA基因的新疆维吾尔自治区塔什库尔干塔吉克自治县采获蜱中无形体最大似然法系统发育树注:◆本研究获得的牛无形体序列。 Fig. 2 Maximum likelihood-based phylogenetic tree of the 16S rRNA gene of Anaplasma in ticks collected from Taxkorgan Tajik Autonomous County, Xinjiang Uygur Autonomous Region, China |