1 材料与方法
1.1 蚊密度数据
1.2 气象数据
1.3 统计分析方法
2 结果
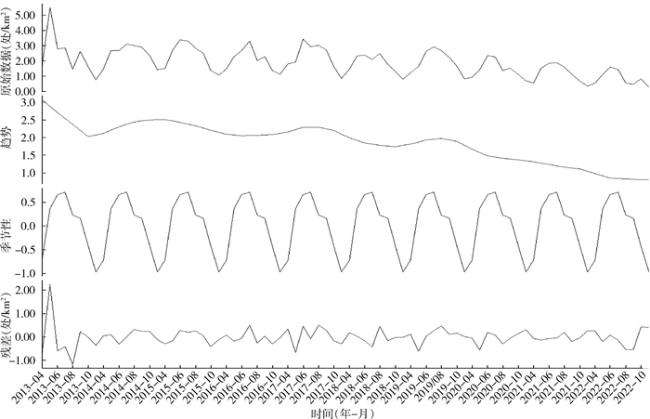
2.1 幼蚊密度基本特征
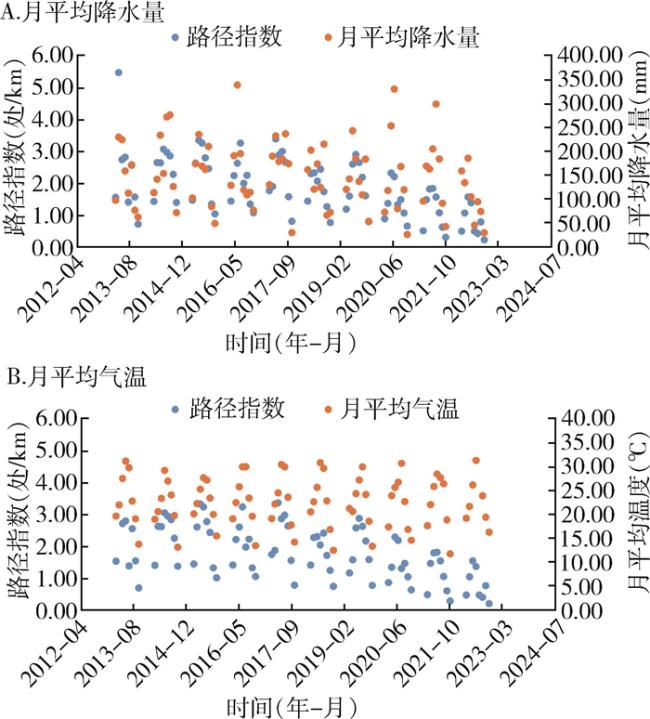
2.2 气象因素基本特征
表1 重庆市2013-2022年4-11月各气象因素的基本特征Tab. 1 Basic characteristics of meteorological factors in Chongqing, China, April to November, 2013-2022 |
| 气象因素 | 均值 | 标准差 | 最小值 | 最大值 | P5 | P25 | P50 | P75 | P95 |
| 累计降水量(mm) | 149.56 | 69.81 | 27.18 | 339.42 | 43.78 | 97.15 | 142.84 | 189.57 | 276.77 |
| 气温(℃) | 22.97 | 5.26 | 11.99 | 34.35 | 13.60 | 19.33 | 22.96 | 27.14 | 31.02 |
| 露点(℃) | 17.57 | 7.18 | 9.45 | 23.78 | 10.26 | 14.82 | 18.38 | 20.95 | 22.87 |
| 海平面气压(hPa) | 1 009.43 | 6.70 | 998.60 | 1 023.26 | 1 000.05 | 1 002.82 | 1 009.26 | 1 015.14 | 1 021.44 |
| 站点气压(hPa) | 981.33 | 10.06 | 959.69 | 1 021.52 | 971.58 | 974.11 | 979.81 | 986.68 | 1 002.12 |
| 风速(m/s) | 4.25 | 0.44 | 3.25 | 5.67 | 3.50 | 3.98 | 4.26 | 4.49 | 4.98 |
| 最大风速(m/s) | 8.90 | 0.92 | 6.90 | 11.14 | 7.29 | 8.27 | 8.84 | 9.64 | 10.46 |
| 最高温度(℃) | 27.42 | 10.75 | 15.56 | 40.91 | 16.13 | 23.53 | 26.91 | 32.31 | 23.36 |
| 最低温度(℃) | 19.33 | 8.56 | 8.76 | 29.08 | 11.46 | 15.89 | 119.66 | 36.08 | 26.56 |
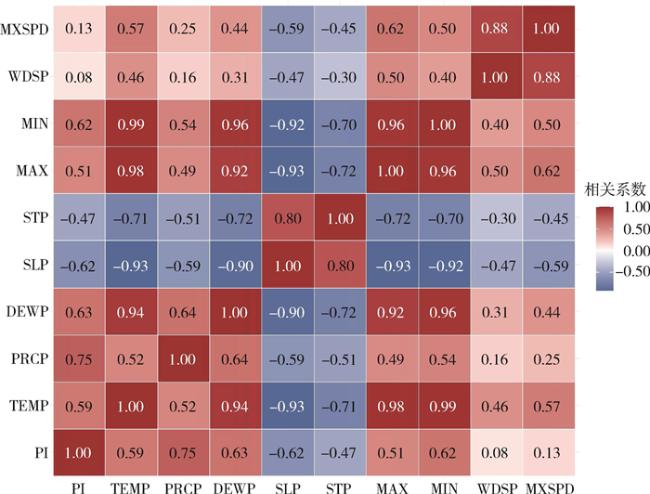
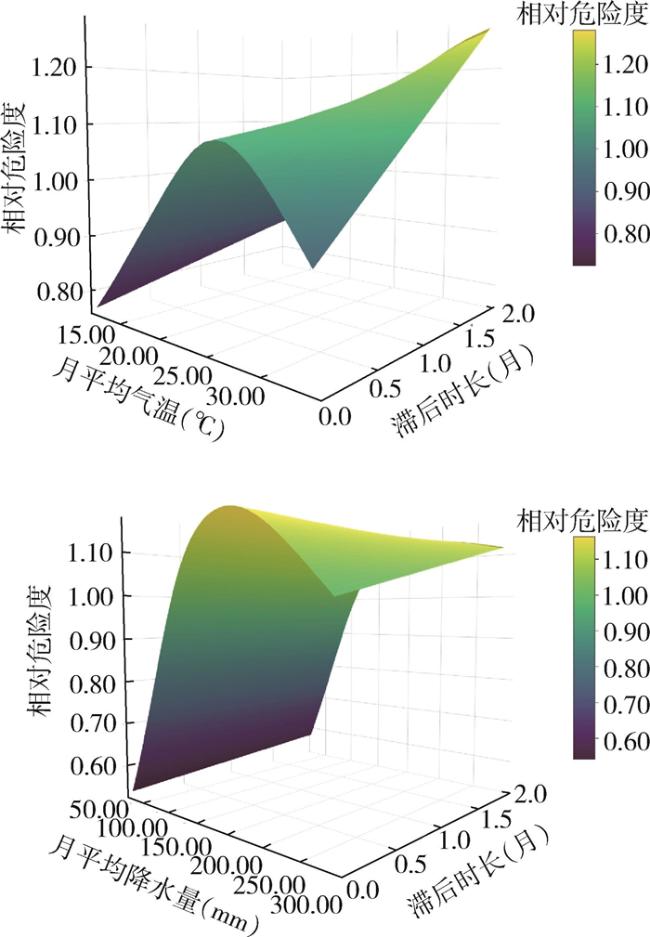
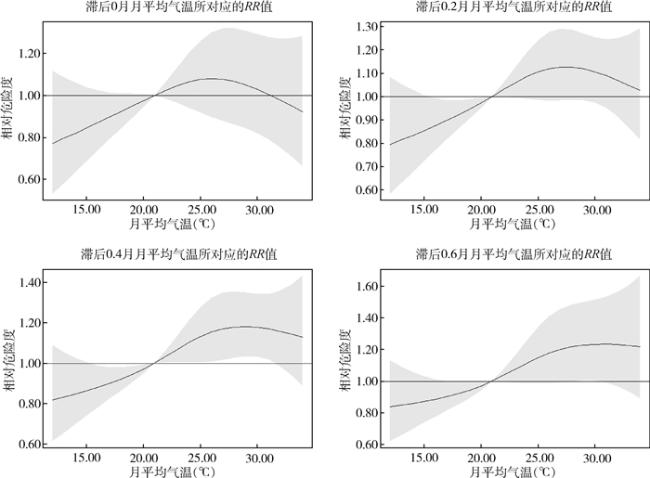
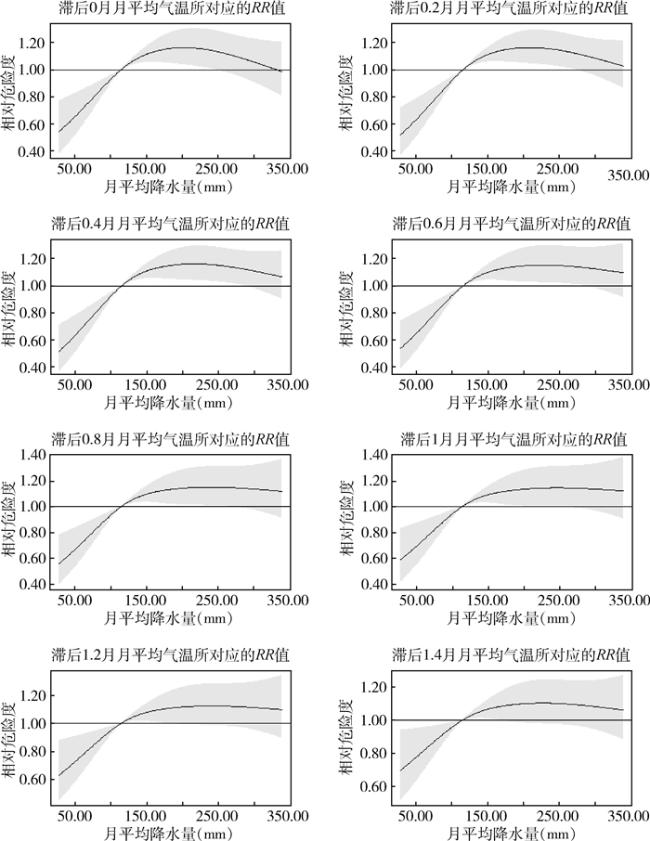
2.3 蚊虫密度与气象因素的相关性分析
图2 重庆市2013-2022年4-11月气象因素与幼蚊密度相关性注:蓝色表示相关系数为负值,红色表示相关系数为正值;MAX最高气温;MXSPD最大风速;WDSP平均风速;STP站点气压;SLP海平面气压;DEWP露点;TEMP平均气温;PRCP月平均降水量;MIN最低气温;PI幼蚊路径指数。 Fig. 2 Correlation between meteorological factors and mosquito larvae density in Chongqing, China, April to November, 2013-2022 |