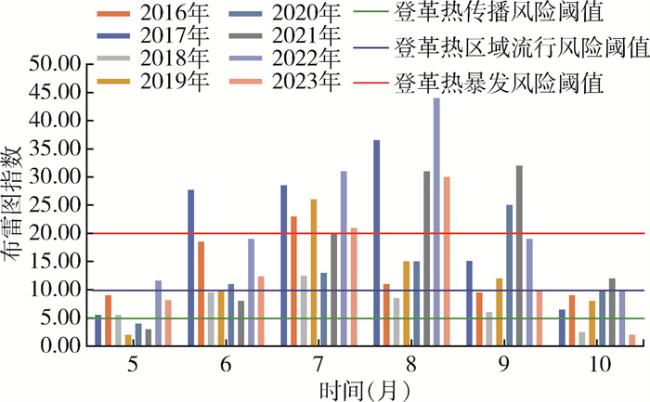
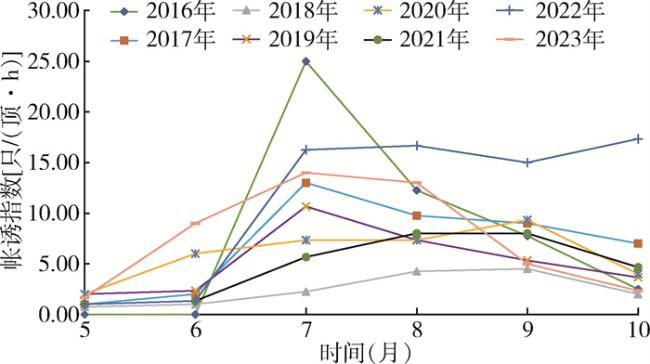
Objective: To investigate the density, seasonality, and resistance to commonly used insecticides of Aedes albopictus populations in Panzhihua, Sichuan Province, China, and analyze regional insecticide application practices, so as to provide evidence-based recommendations for rational insecticide use and dengue fever prevention and control strategies. Methods: From May to October of 2016-2023, Ae. albopictus ecological surveillance was conducted in residential areas, parks, rural houses, and other suitable habitats across Panzhihua, using the double mosquito net method for adults and the Breteau index (BI) method for larvae. Field-collected larval and adult Ae. albopictus specimens were reared together to the F1 generation in the laboratory and the resistance of Ae. albopictus to commonly used insecticides was detected by dipping method for the larvae and the WHO tube bioassay for the adults. Results: From 2016 to 2023 in Panzhihua, Ae. albopictus density features were as following: BI=14.41; container index (CI)=18.53; net trap index=6.49 mosquitoes/(trap∙h); and larval populations all exhibited unimodal seasonal dynamics in 2016-2023, with peak BI values (12.50-44.00) occurring during July to September. The major breeding sites were water storage containers (pools, vats, and basins) and idle containers, with combined positive cases accounting for 44.50% of the tatal positive containers, and positive breeding sites were mostly located in outdoor environments. In 2018, Ae. albopictus larvae were susceptible to dichlorvos [resistance ratio (RR)=0.47], permethrin (RR=1.95), temephos (RR=0.70), deltamethrin (RR=2.20), and beta-cypermethrin (RR=1.15); the RR of beta-cypermethrin and temephos increased slightly, while those of the other three insecticides decreased, as compared with 2015; and in 2022, the RR of beta-cypermethrin rose to 122.51, with resistance level escalating from susceptibility to high resistance whin the five years, while the larvae showed low resistance to propoxur (RR=3.08) and phoxim (RR=3.73). From 2019 to 2022, adult populations showed declined susceptibility to deltamethrin (mortality, from 66.43% to 62.37%); a transition from susceptibility to possible resistance was observed for malathion (mortality, from 100% to 87.78%) and propoxur (mortality, from 100% to 96.47%); and the response to beta-cypermethrin remained at a level of possible resistance (mortality, from 90.08% to 89.77%). Conclusions: Imported dengue cases, high-density mosquitoes, and insecticide resistance development create critical disease control challenges. Ae. albopictus larvae have developed high resistance to beta-cypermethrin, but remain susceptible to organophosphate compounds such as temephos and dichlorvos; and adults remain resistant to deltamethrin and malathion. It is recommended to manage the mosquito breeding sites, reduce the use of pyrethroids with high resistance in chemical control, and rotate the application of sensitive insecticides, so as to enhance Ae. albopictus control effectiveness and delay the development and progression of resistance.