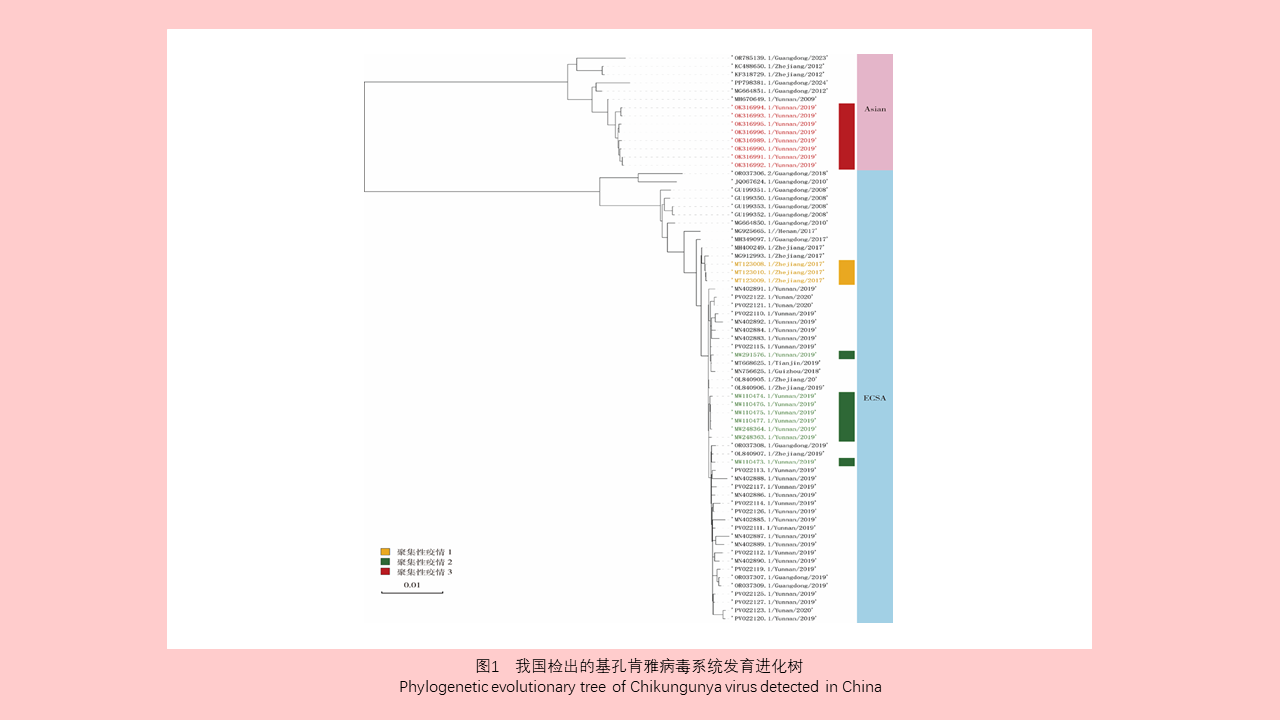
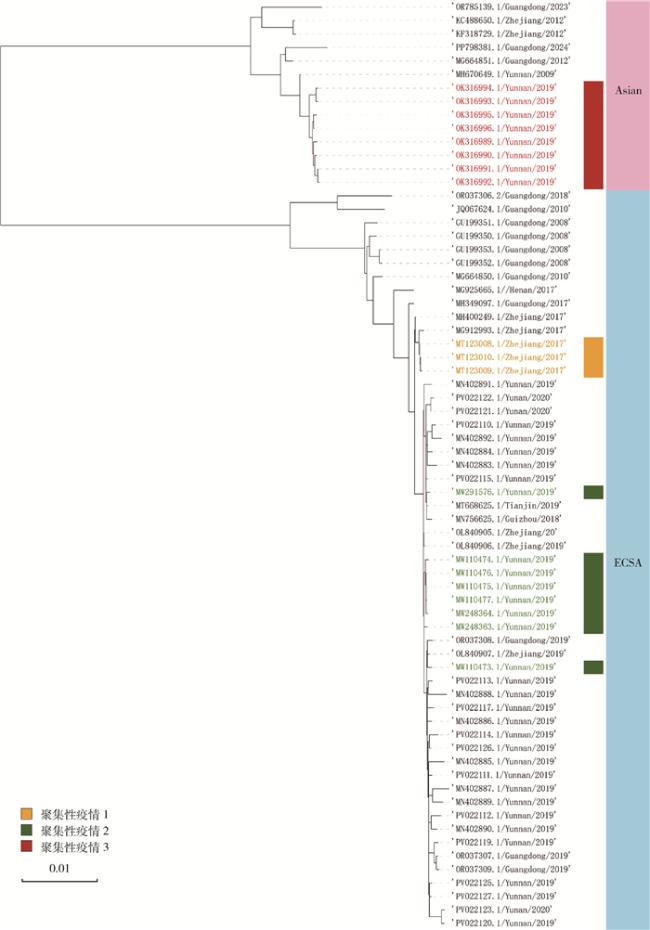
1 引言
2 CHIKV基因型与全球分布
2.1 病毒基因分型与全球分布情况
2.2 各基因型亚洲分布情况
3 我国检出的CHIKV基因型分布特征
3.1 输入性病例基因型溯源
表1 我国输入性基孔肯亚热病例检出的基孔肯雅病毒基因型分布Tab. 1 Genotype distribution of Chikungunya virus detected in imported cases of Chikungunya fever in China |
| 时间(年) | 地点 | 基因型 | 输入国家 | 报告单位 | 报告人及参考文献 |
| 2008 | 广东省广州市 | ECSA | 斯里兰卡 | 广东出入境检验检疫局 | 郑夔等[20] |
| 2008 | 广东省茂名市 | ECSA | 马来西亚 | 广东出入境检验检疫局 | 洪烨等[49] |
| 2009 | 广东省广州市 | ECSA | 印度 | 广东出入境检验检疫局 | 黄鹂等[51] |
| 2010 | 广东省深圳市 | ECSA | 印度 | 深圳市疾病预防控制中心 | 许少坚等[68] |
| 2012 | 广东省深圳市 | Asian | 印度尼西亚 | 深圳市疾病预防控制中心 | 阳帆等[61] |
| 2012 | 浙江省宁波市 | Asian | 菲律宾 | 宁波国际旅行卫生保健中心 | 周冬根和罗洁[69] |
| 2012 | 福建省厦门市 | Asian | 菲律宾 | 福建省疾病预防控制中心 | 黄萌等[66] |
| 2017 | 广东省广州市 | ECSA | 巴基斯坦 | 广州市疾病预防控制中心 | 甄若楠等[62] |
| 2017 | 浙江省温州市 | ECSA | 孟加拉国 | 丽水市疾病预防控制中心 | 王晓光等[55] |
| 2017 | 河南省洛阳市 | ECSA | 斯里兰卡 | 洛阳市疾病预防控制中心 | 李双玲和朱鑫[44] |
| 2017 | 浙江省衢州市 | Asian | 孟加拉国 | 温州市疾病预防控制中心 | 章显传等[65] |
| 2017 | 广东省广州市 | Asian | 孟加拉国 | 广州市疾病预防控制中心 | 甄若楠等[62] |
| 2018 | 重庆市 | ECSA | 泰国 | 重庆国际旅行卫生保健中心 | 文海燕等[45] |
| 2018 | 广东省广州市 | Asian | 印度 | 广州市疾病预防控制中心 | 甄若楠等[62] |
| 2018 | 福建省福州市 | Asian | 菲律宾 | 福建省疾病预防控制中心 | 俞婷婷等[67] |
| 2019 | 云南省昆明市 | ECSA | 泰国 | 昆明理工大学生命科学与技术学院 | 冯悦等[53] |
| 2019 | 云南省昆明市 | ECSA | 缅甸 | 云南省疾病预防控制中心 | 陈瑶瑶等[54] |
| 2019 | 浙江省杭州市 | ECSA | 泰国 | 浙江省疾病预防控制中心 | 张严峻等[56] |
| 2019 | 辽宁省大连市 | ECSA | 缅甸 | 大连海关 | 高玉峰等[46] |
| 2019 | 贵州省遵义市 | ECSA | 缅甸 | 中国人民解放军疾病预防控制中心 | 邱少富等[57] |
| 2019 | 河南省新乡市 | ECSA | 缅甸 | 河南省疾病预防控制中心 | 李幸乐等[58] |
| 2019 | 天津市 | ECSA | 缅甸 | 天津疾病预防控制中心 | 谢彤等[59] |
| 2019 | 湖南省怀化市 | ECSA | 泰国 | 湖南省疾病预防控制中心 | 何方玲等[60] |
| 2019 | 广东省广州市 | Asian | 泰国 | 广州市疾病预防控制中心 | 甄若楠等[62] |
| 2019 | 广东省广州市 | Asian | 缅甸 | 广州市疾病预防控制中心 | 甄若楠等[62] |
| 2019 | 广东省广州市 | Asian | 印度 | 广州市疾病预防控制中心 | 甄若楠等[62] |
| 2023 | 广东省广州市 | Asian | 印度尼西亚 | 广州市疾病预防控制中心 | Su W等上传(OR785139.1)a |
| 2024 | 广东省广州市 | Asian | 东帝汶 | 广州市第八人民医院传染病研究所 | 江梦玲等[63] |
注:a为仅上传至美国国家生物技术信息中心(NCBI)数据库但未发表论文,括号中为GenBank登录号。 |
3.2 输入性病例引发聚集性疫情基因型分布
表2 我国输入性病例引起的本地聚集性基孔肯雅热疫情中的病毒基因型分布Tab. 2 Genotype distribution of local cases of chikungunya fever in the outbreak caused by imported cases in China |
| 时间(年) | 地点 | 基因型 | 事件 | 报告单位 | 报告人及参考文献 |
| 2010 | 广东省东莞市 | ECSA | 由不明来源输入性病例引起的国内首起本地社区暴发疫情(282例) | 东莞市疾病预防控制中心 | 袁达康[70] |
| 2017 | 浙江省衢州市 | ECSA | 由孟加拉国输入性病例引起的聚集性疫情(3例) | 衢州市疾病预防控制中心 | 曹国平等[71] |
| 2019 | 云南省瑞丽市 | ECSA | 由输入性病例引起的聚集性疫情(112例) | 昆明理工大学生命科学与技术学院 | 冯悦等[53] |
| 2019 | 云南省西双版纳 | Asian | 从登革热样发热门诊患者的血清样本检测到CHIKV RNA(88份)a | 中国医学科学院医学生物学研究所和北京协和医学院 | 邹梦等[72] |
| 2025 | 广东省佛山市 | ECSA | 未知来源输入型毒株引起聚集性疫情(> 9 000例) | 广东省疾病预防控制中心 | 李艳等[23] |
注:西双版纳西双版纳傣族自治洲;a本次疫情主要为登革热疫情,基孔肯雅病毒的检测为回顾性调查中发现的登革病毒和基孔肯雅病毒复合感染。 |