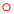1 材料与方法
1.1 样本来源
表1 云南省景洪市野生种群伊蚊采集信息Tab. 1 Information on wild Aedes populations in Jinghong, Yunnan Province |
| 蚊种 | 方向 | 采集地点 | 雌蚊(只) | 雄蚊(只) | 幼蚊(只) | 地理坐标 | 采集时间 |
| 埃及伊蚊 | 东 | 告庄景兰寨 | 16 | 16 | 16 | 22°01'14″N,100°81'68″E | 2023年9月 |
| 告庄景罕寨 | 16 | 16 | 16 | 22°01'15″N,100°81'73″E | 2023年9月 | ||
| 南 | 曼龙匡 | 16 | 16 | 16 | 21°99'06″N,100°81'07″E | 2023年9月 | |
| 曼弄枫 | 16 | 16 | 16 | 21°97'22″N,100°79'85″E | 2023年9月 | ||
| 西 | 万达三期 | 16 | 16 | 16 | 22°02'16″N,100°75'81″E | 2023年9月 | |
| 花卉园小区 | 16 | 16 | 16 | 22°00'96″N,100°78'29″E | 2023年9月 | ||
| 北 | 曼斗村 | 16 | 16 | 16 | 22°01'55″N,100°81'02″E | 2023年8月 | |
| 鑫顺鑫北城 | 16 | 16 | 16 | 22°01'80″N,100°81'20″E | 2023年10月 | ||
| 中 | 景洪城区 | 16 | 16 | 16 | 22°01'65″N,100°79'31″E | 2023年10月 | |
| 龙舟广场 | 16 | 16 | 16 | 22°00'31″N,100°81'06″E | 2023年10月 | ||
| 白纹伊蚊 | - | 景洪 | 32 | 32 | 32 | - | 2023年10月 |
注:- 白纹伊蚊为多采样点混合样品,未记录经纬度信息。 |
1.2 蚊虫基因组DNA提取及wsp基因扩增和测序
1.3 系统发育分析
1.4 统计学分析
2 结果
2.1 埃及伊蚊和白纹伊蚊沃尔巴克氏体自然感染比较
表2 云南省景洪市不同方位、虫态和性别埃及伊蚊沃尔巴克氏体自然感染情况Tab. 2 The status of natural infection with Wolbachia in Aedes aegypti by geographical orientation, developmental stage, and sex in Jinghong, Yunnan Province |
| 采集 方位 | 雌蚊 | 雄蚊 | 幼蚊 | 总计 | |||||||
| 检出样本数(份) | 检出率(%) | 检出样本数(份) | 检出率(%) | 检出样本数(份) | 检出率(%) | 检出样本数(份) | 检出率(%) | ||||
| 东 | 1 | 3.13 | 4 | 12.50 | 0 | 0.00 | 5 | 5.21 | |||
| 南 | 1 | 3.13 | 1 | 3.13 | 0 | 0.00 | 2 | 2.08 | |||
| 西 | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 | |||
| 北 | 1 | 3.13 | 1 | 3.13 | 2 | 6.25 | 4 | 4.17 | |||
| 中 | 1 | 3.13 | 1 | 3.13 | 4 | 12.50 | 6 | 6.25 | |||
| 合计 | 4 | 2.50 | 7 | 4.38 | 6 | 3.75 | 17 | 3.54 | |||
注:不同采集方位雌、雄和幼蚊的检测样本数量均为32只。 |
表3 云南省景洪市不同虫态、性别埃及伊蚊和白纹伊蚊wAlbA,wAlbB及wAlbA+wAlbB自然感染情况Tab. 3 The status of natural infection with wAlbA, wAlbB, and wAlbA+wAlbB in Aedes aegypti and Ae. albopictus by developmental stage and sex in Jinghong, Yunnan Province |
| 蚊种 | 虫态/性别 | 检测数 (份) | 检出率 (%) | wAlbA | wAlbB | wAlbA+wAlbB | |||||
| 检出样本数 (份) | 构成比 (%) | 检出样本数 (份) | 构成比 (%) | 检出样本数 (份) | 构成比 (%) | ||||||
| 埃及伊蚊 | 雌蚊 | 4 | 2.50 | 3 | 75.00 | 0 | 0.00 | 1 | 25.00 | ||
| 雄蚊 | 7 | 4.38 | 0 | 0.00 | 1 | 14.29 | 6 | 85.71 | |||
| 幼蚊 | 6 | 3.75 | 3 | 50.00 | 2 | 33.33 | 1 | 16.67 | |||
| 合计 | 17 | 3.54 | 6 | 35.29 | 3 | 17.65 | 8 | 47.06 | |||
| 白纹伊蚊 | 雌蚊 | 31 | 96.86 | 3 | 9.68 | 1 | 3.22 | 27 | 87.10 | ||
| 雄蚊 | 29 | 90.63 | 3 | 10.34 | 1 | 3.45 | 25 | 86.21 | |||
| 幼蚊 | 29 | 90.63 | 3 | 10.34 | 0 | 0.00 | 26 | 89.66 | |||
| 合计 | 89 | 92.71 | 9 | 10.11 | 2 | 2.25 | 78 | 87.64 | |||
注:检测数即各类型样本中的沃尔巴克氏体阳性数,检出率即沃尔巴克氏体检出率。 |
2.2 不同虫态和性别埃及伊蚊和白纹伊蚊沃尔巴克氏体自然感染
2.3 埃及伊蚊和白纹伊蚊wAlbA+wAlbB共感染比较
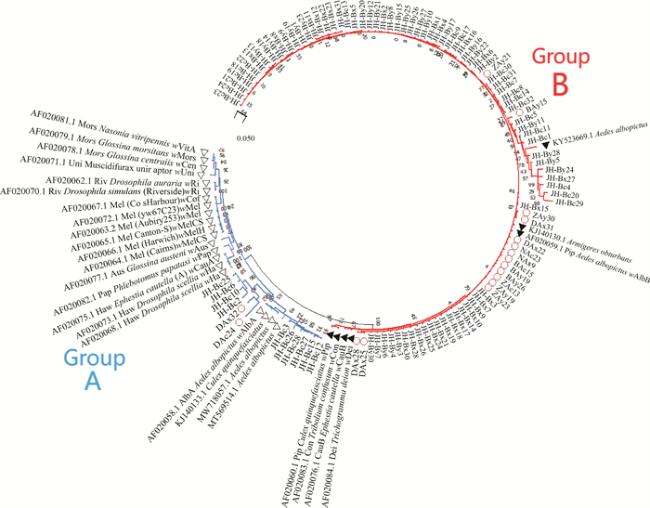
2.4 沃尔巴克氏体wsp基因序列系统发育分析
2.5 埃及伊蚊和白纹伊蚊沃尔巴克氏体wsp基因单倍型分析
表4 云南省景洪市埃及伊蚊和白纹伊蚊中沃尔巴克氏体wsp基因单倍型信息Tab. 4 Information on Wolbachia surface protein gene (wsp) haplotypes in Aedes aegypti and Ae. albopictus in Jinghong, Yunnan Province |
| 超群 | 单倍型 | 基因序列数 | 宿主 |
| A | H1 | 1 | 埃及伊蚊 |
| H4 | 2 | 埃及伊蚊、白纹伊蚊 | |
| H10 | 1 | 白纹伊蚊 | |
| H13 | 1 | 白纹伊蚊 | |
| H14 | 1 | 白纹伊蚊 | |
| H17 | 1 | 白纹伊蚊 | |
| H18 | 2 | 白纹伊蚊 | |
| B | H2 | 39 | 埃及伊蚊、白纹伊蚊 |
| H3 | 1 | 埃及伊蚊 | |
| H5 | 6 | 埃及伊蚊、白纹伊蚊 | |
| H6 | 1 | 埃及伊蚊 | |
| H7 | 1 | 埃及伊蚊 | |
| H8 | 21 | 埃及伊蚊、白纹伊蚊 | |
| H9 | 19 | 埃及伊蚊、白纹伊蚊 | |
| H11 | 3 | 白纹伊蚊 | |
| H12 | 1 | 白纹伊蚊 | |
| H15 | 1 | 白纹伊蚊 | |
| H16 | 1 | 白纹伊蚊 | |
| H19 | 1 | 白纹伊蚊 | |
| H20 | 1 | 白纹伊蚊 | |
| H21 | 1 | 白纹伊蚊 |